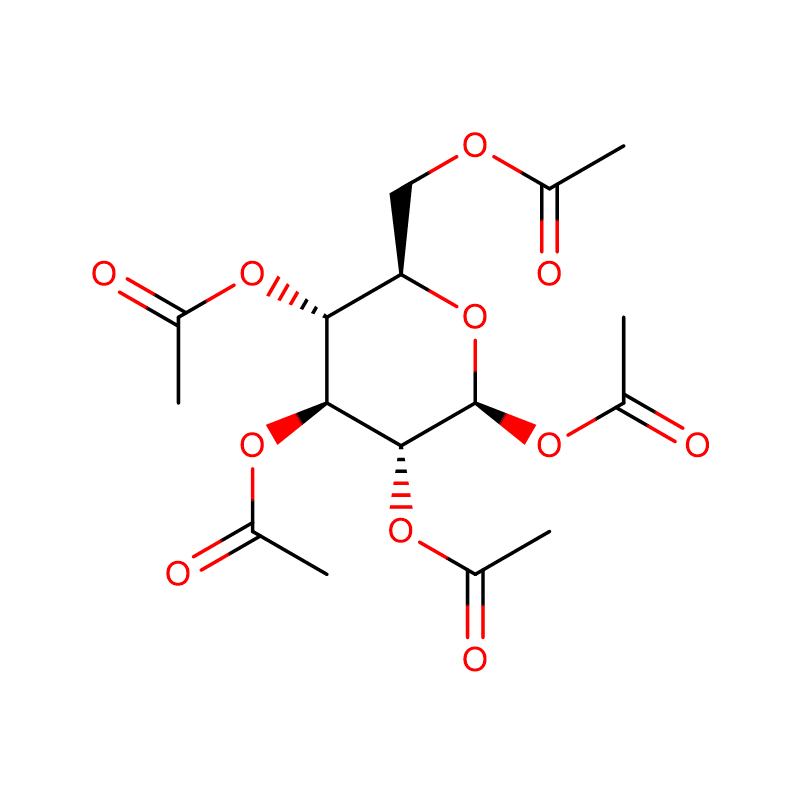
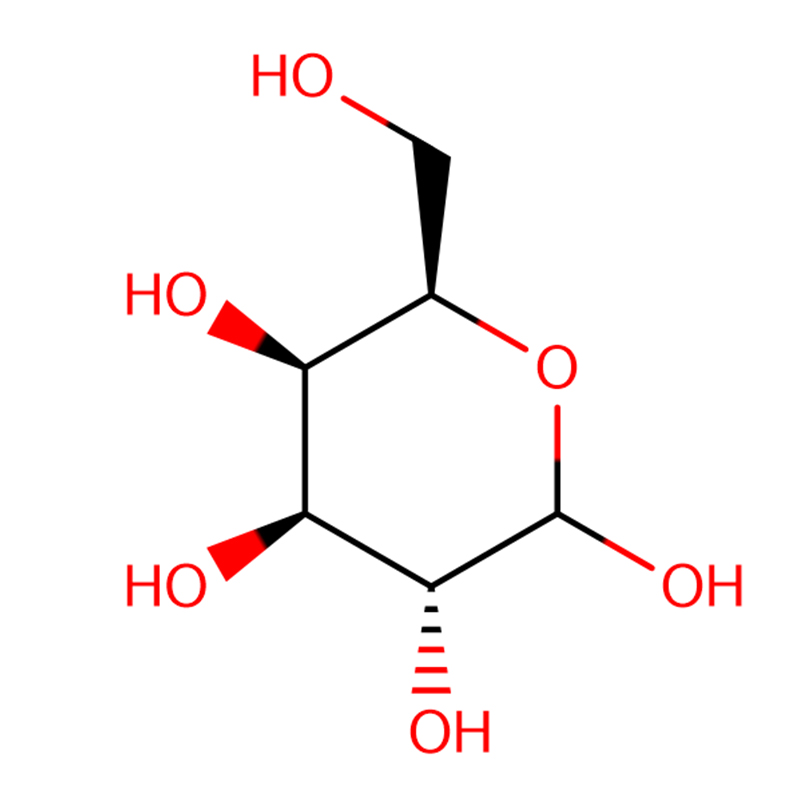
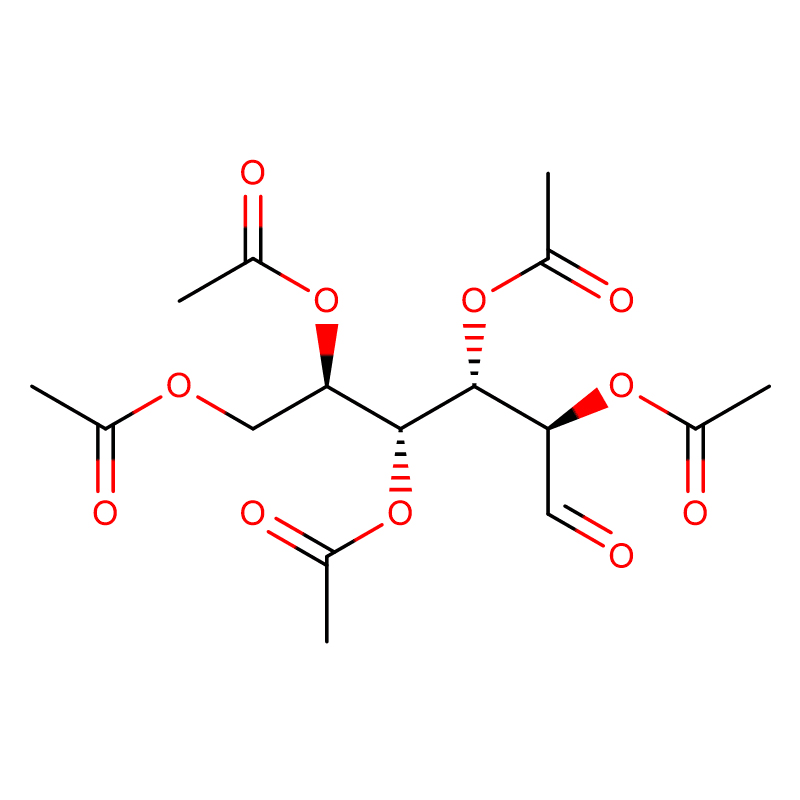
4-NITROFENIL-ALFA-D-MANOPIRANOZID CAS: 10357-27-4 Pulbere alb murdar 98%
| Număr de catalog | XD90011 |
| numele produsului | 4-nitrofenil-alfa-D-manopiranozidă |
| CAS | 10357-27-4 |
| Formulă moleculară | C12H15NO8 |
| Greutate moleculară | 30301.25 |
| Detalii de depozitare | -2la -8°C |
| Cod tarifar armonizat | 29400000 |
Specificatiile produsului
| Apă | <5% Karl Fische |
| Solubilitate | 1% în DMF este limpede și incolor |
| Puritate | 4-nitrofenol liber <200 ppm |
| HPLC | >98% |
| Aspect | Pulbere alb murdar |
Perspective mecaniciste asupra unei familii de alfa-manozidaze dependente de Ca2+ într-un simbiont intestinal uman.
Bacteriile colonice, exemplificate de Bacteroides thetaiotaomicron, joacă un rol cheie în menținerea sănătății umane prin valorificarea familiilor mari de glicozide hidrolaze (GH) pentru a exploata polizaharidele dietetice și glicanii gazdă ca nutrienți.O astfel de expansiune a familiei GH este exemplificată prin familia de 23 de glicozidaze GH92 codificate de genomul B. thetaiotaomicron.Aici arătăm că acestea sunt alfa-manozidaze care acționează printr-un singur mecanism de deplasare pentru a utiliza N-glicanii gazdă.Structura tridimensională a două manozidaze GH92 definește o familie de proteine cu două domenii în care centrul catalitic este situat la interfața domeniului, oferind asistență acidă (glutamat) și bazică (aspartat) la hidroliză într-un Ca(2+)- mod dependent.Structurile tridimensionale ale GH92 în complex cu inhibitori oferă o perspectivă asupra specificității, mecanismului și itinerariului conformațional al catalizei.Ca(2+) joacă un rol catalitic cheie în a ajuta la distorsionarea manozidei de la starea sa fundamentală (4)C(1) conformației scaunului către starea de tranziție.(Bibliografie: Nat.Chim.Biol.6, 125-32, (2010)
Cromatografia de afinitate frontală a glicoasparaginelor de ovalbumină pe o coloană de concanavalin A-sefaroză.Un studiu cantitativ al specificității de legare a lectinei.
Interacțiunile concanavalinei A (ConA) imobilizate cu Sepharose 4B cu 10 glicoasparagine derivate din ovalbumină au fost investigate cantitativ prin cromatografie de afinitate frontală.În această metodă, o soluție de carbohidrați este aplicată continuu pe o coloană ConA-Sepharose și întârzierea frontului de eluție este măsurată ca parametru al puterii interacțiunii.Se poate determina constanta de disociere (Kd) pentru fiecare zaharidă cu ConA.O analiză a legării p-nitrofenil-alfa,D-manozidei a arătat că proprietățile de legare ale ConA nu se modifică în mod esențial după imobilizarea pe Sepharose 4B.Fiecare dintre glicoasparaginele de ovalbumină a fost marcată cu tritiu prin metoda de metilare reductivă pentru analiză.O comparație a valorilor Kd obținute a arătat că legarea ConA variază considerabil cu diferențe structurale foarte mici ale lanțului glicozilic.Rezultatele sugerează că ConA recunoaște o structură specifică a lanțului glicozilic, Man alfa 1-6(Man alfa 1-3)Man, în care cel puțin o grupare hidroxil la poziția C-3 a manozei legate de C-6 ar trebui să fie liberă.