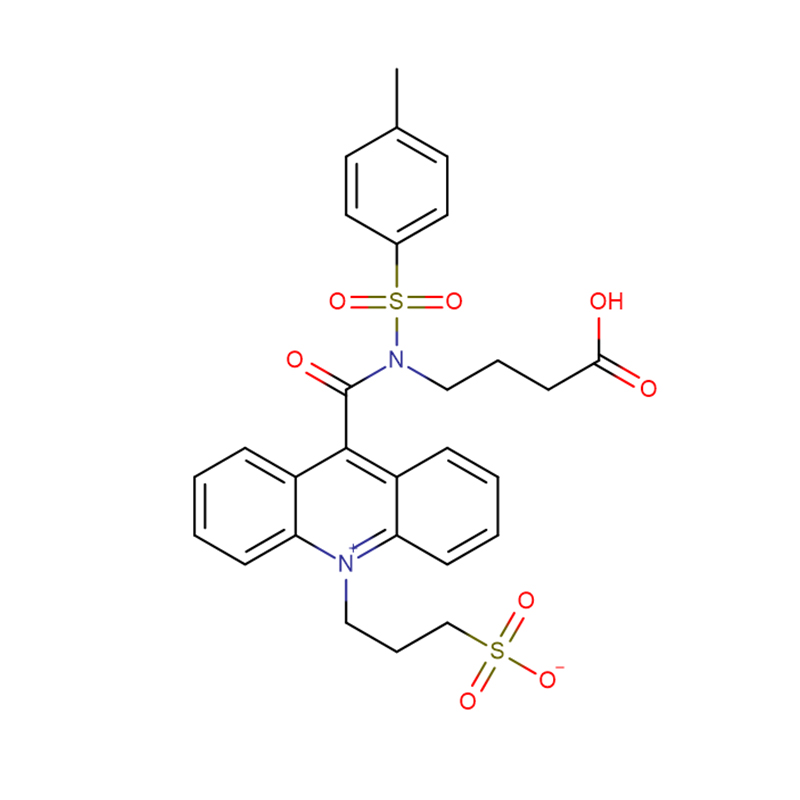
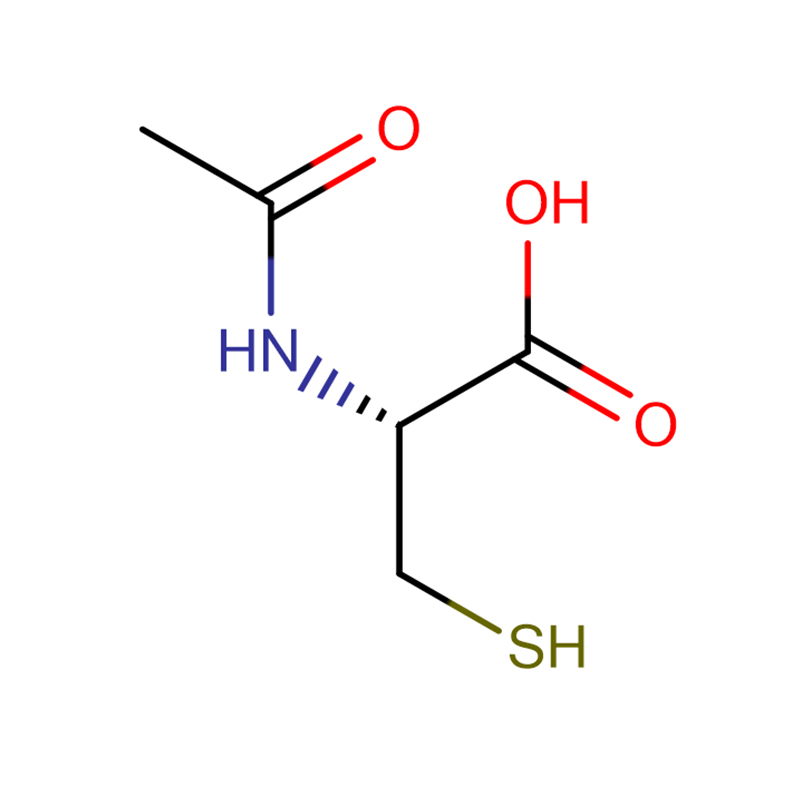
4-Amino-3-hidrazino-1,2,4-triazol-5-tiol Cas:28836-03-5 99% Solid galben până la verde
| Număr de catalog | XD90146 |
| numele produsului | 4-amino-3-hidrazino-1,2,4-triazol-5-tiol |
| CAS | 28836-03-5 |
| Formulă moleculară | C16H13NO3S.NH3 |
| Greutate moleculară | 316,37 |
| Detalii de depozitare | Înconjurător |
| Cod tarifar armonizat | 2923900090 |
Specificatiile produsului
| Aspect | Solid galben până la verde |
| Assay | ≥ 99% |
| Punct de topire | 237°C(dec.)(lit.) |
| Solubilitate | NaOH: solubil 1 N |
| Solubil în apă | Solubil în apă, NaOH 1 N și metanol. |
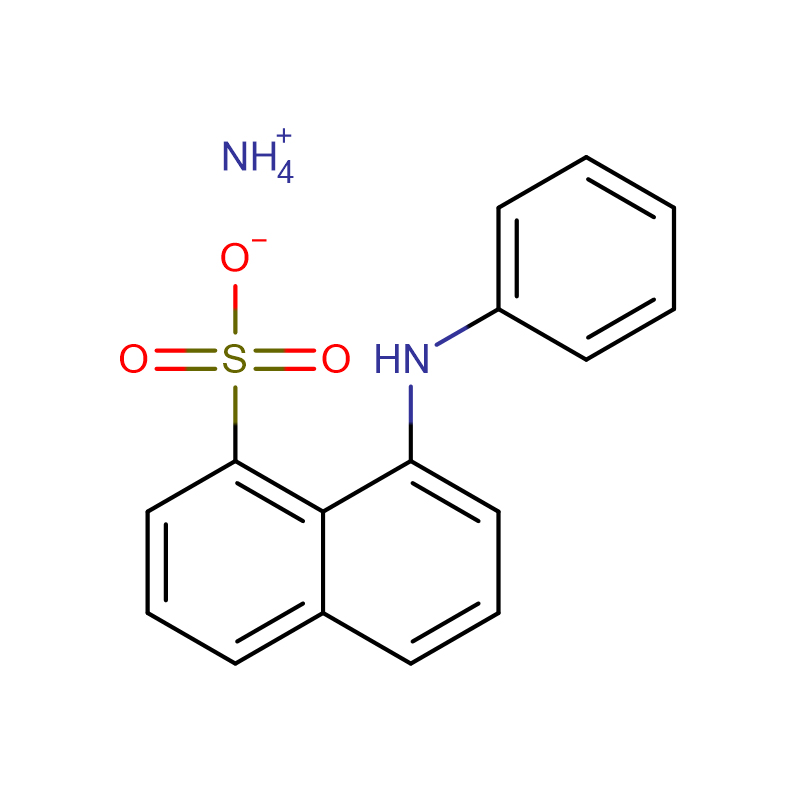
1. Am studiat efectele inhibitoare ale izorhamnetinei asupra tirozinazei ciupercilor prin cinetica de inhibiție și simulare computațională.Isorhamnetina a inhibat reversibil tirozinaza într-o manieră de tip mixt la Ki=0,235±0,013 mM.Măsurătorile fluorescenței intrinseci și de legare la 1-anilinonaftalen-8-sulfonat (ANS) au arătat că izorhamnetina nu a indus modificări semnificative în structura terțiară a tirozinazei.Pentru a obține o perspectivă asupra procesului de inactivare, cinetica a fost calculată prin măsurători cu interval de timp și reacții continue pe substrat.Rezultatele au indicat că inactivarea indusă de izorhamnetină a fost o reacție de ordinul întâi cu procese bifazice.Pentru a obține mai multe informații, am simulat andocarea între tirozinază și izorhamnetină.Simularea a avut succes (energii de legare pentru Dock6.3: -32,58 kcal/mol, pentru AutoDock4.2: -5,66 kcal/mol și pentru Fred2.2: -48,86 kcal/mol), sugerând că izorhamnetina interacționează cu mai multe reziduuri, cum ar fi ca HIS244 și MET280.Această strategie de predicție a interacțiunii tirozinazei în combinație cu cinetica bazată pe un compus de flavanonă s-ar putea dovedi utilă în depistarea potențialilor inhibitori naturali ai tirozinazei.
2. Calea de desfășurare a acidului a conalbuminei (CA), o glicoproteină monomerică din albușul de ou de găină, a fost investigată folosind spectroscopie CD departe și aproape UV, emisie de fluorescență intrinsecă, sonda de fluorescență extrinsecă 1-anilino-8-naftalen sulfonat (ANS) și împrăștierea dinamică a luminii (DLS).Observăm modificări dependente de pH în structura secundară și terțiară a CA.Are o structură secundară α-helicală asemănătoare nativă la pH 4,0, dar o structură de pierdere la pH 3,0.CA a existat exclusiv ca stare de globule pre-topit și stare de globule topit în soluție la pH 4,0 și, respectiv, pH 3,0.Efectul pH-ului asupra conformației și termostabilității CA indică rezistența la căldură la pH neutru.Rezultatele DLS arată că starea MG a existat ca formă compactă în soluții apoase cu raze hidrodinamice de 4,7 nm.Stingerea fluorescenței triptofanului de către acrilamidă a confirmat în continuare acumularea unei stări intermediare, parțial desfășurată, între stările native și nepliate.




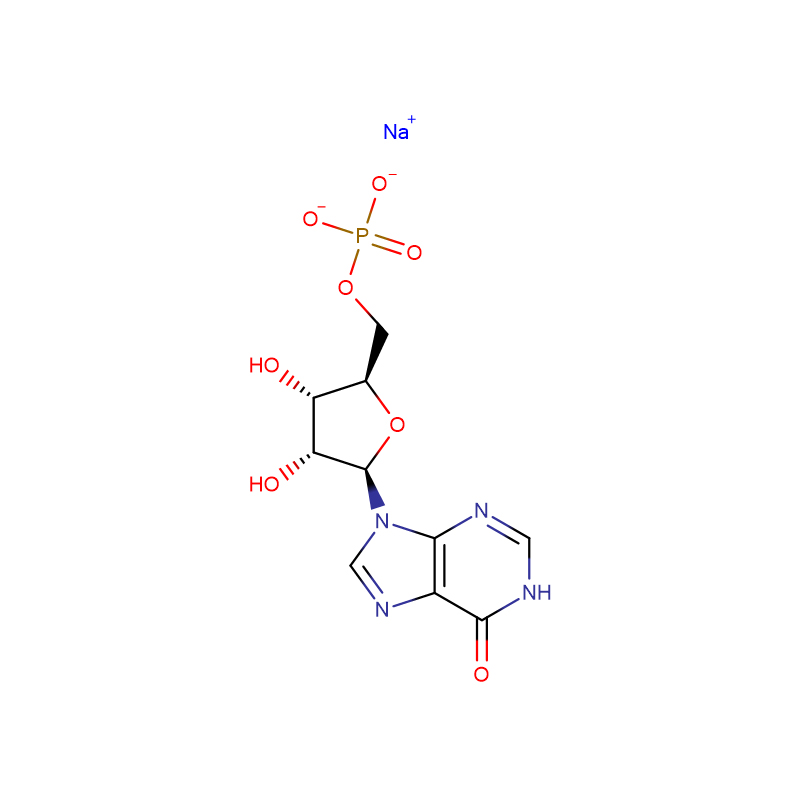
![N-[[bis[4-(dimetilamino)fenil]amino]carbonil] glicină sare de sodiu Pulbere cristalină de culoare albă până la gri-verde](http://cdn.globalso.com/xdbiochems/115871-19-7.jpg)